01.10.2020
 Нанометровые неоднородности – ключ к аномальным свойствам воды
Нанометровые неоднородности – ключ к аномальным свойствам воды
Одной из наиболее интенсивно изучаемых фундаментальных проблем воды является вопрос о существовании структурных неоднородностей (СН) в воде. Ряд исследователей поддерживает возможность существования структурных неоднородностей, однако другие исследователи убеждены в обратном. По данной тематике было выпущено множество экспериментальных и теоретических работ, однако окончательного ответа не было найдено и вопрос оставался открытым.
Международная группа учёных в соавторстве со специалистами лаборатории спектроскопии конденсированных сред Института автоматики и электрометрии СО РАН опубликовала статью [1] в одном из самых авторитетных общенаучных журналов – Scientific Reports, входящем в группу Nature. Для решения фундаментальной задачи авторы предложили оригинальный подход к описанию структуры воды. В рамках этого подхода было показано отсутствие стабильных структурных неоднородностей и постоянное присутствие динамических СН. Результаты этой работы важны для описания природы более чем 50 различных аномальных свойств воды.
В своей работе авторы рассматривают воду как динамическую сеть связей между молекулами, расстояние между которыми не превышает 3,2 ангстрема (Å). С помощью метода молекулярной динамики и структурного анализа изучаются временная и температурная зависимости взаимного расположения каждой пары соседних молекул и энергия взаимодействия между ними. Авторы демонстрируют, что для каждой температуры число водородных связей в системе и координационное число молекул сохраняются во времени и изменяются вблизи среднего значения: сетка водородных связей постоянно перестраивается, однако в любой момент времени включает в себя все молекулы воды. Показано, что для описания природы воды среди прочих её характеристик, зависящих от температуры, можно выделить и число водородных связей (H-связей). При исследовании их энергии обнаружено, что энергия большинства водородных связей значительно превышает тепловую энергию, поэтому, учитывая, что большинство молекул участвуют в образовании четырёх водородных связей, можно говорить о высокой стабильности сформированной сетки, это позволяет жидкой воде проявлять свойства твёрдого тела. При тепловом движении взаимная ориентация молекул может изменяться, водородные связи будут образовываться и распадаться. Небольшая доля связей, энергия которых сравнима с тепловой энергией, ответственна за реорганизацию структуры воды и, соответственно, поведение воды как жидкости. Изменение взаимной ориентации молекул друг относительно друга возможно также под действием внешних электромагнитных сил, которые, следовательно, также могут влиять на свойства воды.
В результате расчётов была обнаружена неоднородность структуры воды, сформированная группами молекул, объединённых более короткими водородными связями. Размер, количество и общая доля вовлечённых молекул зависят от температуры, их пространственное положение со временем изменяется. Каждая неоднородность имеет конечное время жизни и изменчивую структуру, однако такие неоднородности присутствуют в воде в любой момент времени, т. е. всегда.
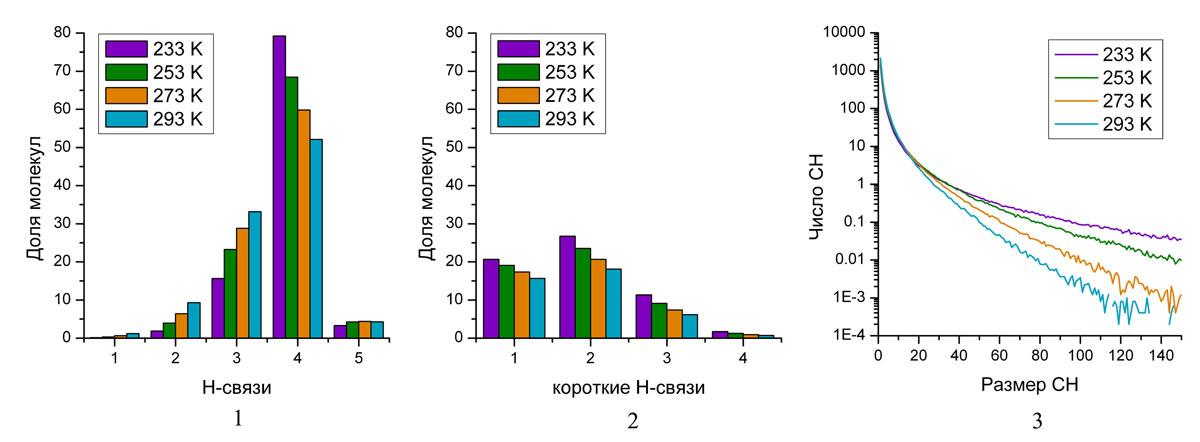
(1) Доли молекул от общего числа, участвующих в образовании 1, 2, 3, 4 и 5 водородных связей (H-связей) при различных температурах. Наблюдается небольшое число молекул, участвующих в образовании 5 связей, что обосновано выбором геометрического критерия H-связи. (2) Доли молекул от общего числа, участвующих в образовании как минимум 1, 2, 3 и 4 коротких H-связей. (3) Распределение усреднённого по времени моделирования числа структурных неоднородностей (СН) в зависимости от числа молекул, образующих эти СН, присутствующих в системе из 8000 молекул воды в любой момент времени. Значения меньше 1 указывают на то, что неоднородности данного размера присутствуют в системе не в любой момент времени.
Таким образом, данное исследование даёт новое представление о воде как о неоднородной динамической системе, состоящей из водородных связей молекул воды, число которых постоянно. Результаты работы разрешают спор о существовании или не существовании неоднородности воды: структура воды обладает динамическими неоднородностями. Учёт рассмотренных в статье новых характеристик важен при исследовании природы макроскопических свойств воды, т. к. открывает новую возможность для описания аномальных свойств, чего раньше окончательно и достоверно сделано не было. Как авторы показали ранее [2], обнаруженные нанонеоднородности могут быть ответственны за неаррениусовское поведение воды при температуре ниже 0 °С.
[1] The nano-structural inhomogeneity of dynamic hydrogen bond network of TIP4P/2005 water // ScientificReports (2020) Vol. 10, Article number:7323, https://doi.org/10.1038/s41598-020-64210-1
[2] Происхождение аномалии поведения вязкости воды вблизи 0 °C // Письма в ЖЭТФ. Т. 102, вып. 11. С. 843.
Материал в формате pdf